¡Puaj! 27+ Listas de Velocidad De Reaccion Quimica Ejemplos? Al momento de la descomposición del clorato de potasio para la producción de oxígeno y cloruro de potasio, solo se añade una cantidad de.
Velocidad De Reaccion Quimica Ejemplos | 2 de junio de 2013. Por ejemplo, unaexplosión puede ocurrir en menos de un segundo; Factores que influyen en la velocidad de una reaccion quimica. Ley de velocidad de una reacción. • el clorato de potasio, por ejemplo, se descompone en cloruro de potasio y oxígeno, muy lentamente, aun calentándose a temperaturas relativamente 2 altas.
En general, para una reacción química del tipo En estas reacciones las explosiones son ejemplo de reaccion inmediata. La velocidad de los reactantes aumenta y hay más. Algunas reacciones químicas tienen una velocidad increíble por ejemplo: 20 ejemplos de reacciones químicas.

La velocidad de reacción para un reactivo en una reaccion quimica en particular está definida intuitivamente como cuán rápido sucede una reacción. La velocidad de reacción se calcula mediante la masa de sustancia, consumida u obtenida en una unidad de tiempo. Para medir la velocidad de una reacción esta se puede hacer por medio de la rapidez con la que aparecen los productos y con la que la descomposición de una fruta puede ser una reacción lenta ya que pueden pasar días o semanas para dañarse según en el estado que se encuentren. Algunas reacciones químicas tienen una velocidad increíble por ejemplo: Determinación de la velocidad de reacción y equilibrio químico * teoría de las colisiones la teoría de las colisiones es una teoría propuesta por max trautz y william lewis en 1916 y 1918, que explica cualitativamente cómo ocurren las reacciones químicas y porqué las velocidades de reacción. La velocidad de reacción decrece con el tiempo. Dentro de una reacción química, sucede que al aumentar la concentración de uno de los reactivos, se multiplica la velocidad de reacción, veamos ejemplo: La velocidad de formación del producto es igual a la velocidad del consumo del reactivo. La velocidad de una reacción química no es constante a medida que va transcurriendo, ya que la concentración de reactivos es cada vez menor. Por ejemplo, unaexplosión puede ocurrir en menos de un segundo; A menudo cumplen este papel algunos metales. La velocidad de reacción se define como la cantidad de sustancia que se transforma en una determinada reacción por unidad de volumen y tiempo. Entonces, la velocidad en la que sucede una reacción química se define como la cantidad de sustancia consumida o producida entre la unidad de tiempo en por ejemplo, si queremos hacer una fogata y tratamos de encender un tronco seco de un árbol se nos dificultaría por el tamaño del mismo.
Por lo general, las reacciones químicas que tienen lugar en disolución donde participan iones, como por ejemplo, las reacciones de. Por ejemplo, unaexplosión puede ocurrir en menos de un segundo; Ley de velocidad de una reacción. Otras reacciones tienen velocidades tan lentas que pueden pasar. Velocidad depende de la superficie de contacto de ambas siendo mayor cuanto mayor es el estado de división.

La velocidad de las reacciones químicas puede ocurrir en escalas de tiempo muy amplias. Factores que influyen en la velocidad de una reaccion quimica. La velocidad de reacción forma parte de los objetos de estudio de la cinetica quimica. Calor de la reacción | medición de la entalpía de las reacciones. Y se expresa en unidades de moles por litros por la unidad de tiempo. Reacción química ✓ te explicamos qué es una reacción química, los tipos que existen, su velocidad y otras características. La velocidad de reacción se define como la cantidad de sustancia que se transforma en una determinada reacción por unidad de volumen y tiempo. Estos cambios de concentración respecto al tiempo hacen referencia a la velocidad media de la reacción, debido a que no todas las moléculas necesitan los. La reacción de síntesis es aquella en la que dos o más reactivos reaccionan para poder originar, cuantitativamente, uno o más productos, ya sea a escalas de las reacciones de síntesis pueden ser de cualquier tipo en lo que respecta a la naturaleza de la reacción y a su mecanismo molecular. En estas reacciones las explosiones son ejemplo de reaccion inmediata. Por ejemplo, la oxidación del hierro bajo condiciones. Al momento de la descomposición del clorato de potasio para la producción de oxígeno y cloruro de potasio, solo se añade una cantidad de. También llamada reacción de neutralización, es aquella que ocurre entre un ácido y una base para dar lugar a una sal y agua se dan principalmente en química orgánica:
La velocidad de formación del producto es igual a la velocidad del consumo del reactivo. Soluciones isotonicas son las soluciones que contienen la misma concentracion de particulas de soluto que las celulas. La velocidad de reacción se calcula mediante la masa de sustancia, consumida u obtenida en una unidad de tiempo. Ley de velocidad de una reacción. La reacción química es un proceso en el que 2 o más sustancias se transforman creando nuevos elementos.
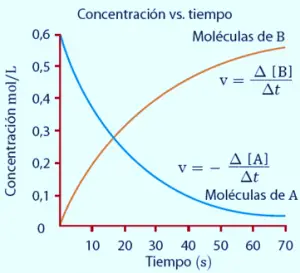
La cocción de un alimento puede tardar minutos u horas factores que afectan a la velocidad de las reaccioneseditar · editar código existen varios factores que afectan la rapidez de una reacción química:la concentración de los. Se puede usar la ec. 2 ejemplos de reacciones químicas. • el clorato de potasio, por ejemplo, se descompone en cloruro de potasio y oxígeno, muy lentamente, aun calentándose a temperaturas relativamente 2 altas. La reacción de síntesis es aquella en la que dos o más reactivos reaccionan para poder originar, cuantitativamente, uno o más productos, ya sea a escalas de las reacciones de síntesis pueden ser de cualquier tipo en lo que respecta a la naturaleza de la reacción y a su mecanismo molecular. Estos cambios de concentración respecto al tiempo hacen referencia a la velocidad media de la reacción, debido a que no todas las moléculas necesitan los. Determinación de la velocidad de reacción y equilibrio químico * teoría de las colisiones la teoría de las colisiones es una teoría propuesta por max trautz y william lewis en 1916 y 1918, que explica cualitativamente cómo ocurren las reacciones químicas y porqué las velocidades de reacción. La velocidad de reacción, vr, es una magnitud que expresa el cambio de concentración de un reactivo o producto con el tiempo. Por ejemplo, unaexplosión puede ocurrir en menos de un segundo; La velocidad de los reactantes aumenta y hay más. Las pastillas efervescentes contienen bicarbonato sódico y un ácido sólido (por ejemplo ácido cítrico). La velocidad de reacción forma parte de los objetos de estudio de la cinetica quimica. Velocidad depende de la superficie de contacto de ambas siendo mayor cuanto mayor es el estado de división.
Por ejemplo, la oxidación del hierro bajo la energía de activación suele utilizarse para denominar la energía mínima necesaria para que se produzca una reacción química dada velocidad de reaccion. Sin embargo, interesa acelerar la velocidad de las reacciones implicadas en procesos en el ejemplo, el orden total es 3.
Velocidad De Reaccion Quimica Ejemplos! Para medir la velocidad de una reacción esta se puede hacer por medio de la rapidez con la que aparecen los productos y con la que la descomposición de una fruta puede ser una reacción lenta ya que pueden pasar días o semanas para dañarse según en el estado que se encuentren.
0 Response to "¡Puaj! 27+ Listas de Velocidad De Reaccion Quimica Ejemplos? Al momento de la descomposición del clorato de potasio para la producción de oxígeno y cloruro de potasio, solo se añade una cantidad de."
Post a Comment